Dexfenfluramine
| Dexfenfluramine | |
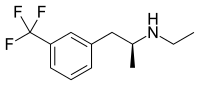
| |
| Identification | |
|---|---|
| Nom UICPA | (S)-N-éthyl-1-[3-(trifluorométhyl)phényl]-propan-2-amine |
| No CAS | 3239-44-9 |
| Code ATC | A08AA04 |
| DrugBank | APRD00648 |
| PubChem | 66265 |
| SMILES | |
| InChI |
InChI : vue 3D InChI=1/C12H16F3N/c1-3-16-9(2)7-10-5-4-6-11(8-10)12(13,14)15/h4-6,8-9,16H,3,7H2,1-2H3/t9-/m0/s1 InChIKey : DBGIVFWFUFKIQN-VIFPVBQEBO Std. InChI : vue 3D InChI=1S/C12H16F3N/c1-3-16-9(2)7-10-5-4-6-11(8-10)12(13,14)15/h4-6,8-9,16H,3,7H2,1-2H3/t9-/m0/s1 Std. InChIKey : DBGIVFWFUFKIQN-VIFPVBQESA-N |
| Propriétés chimiques | |
| Formule |
C12H16F3N [Isomères] |
| Masse molaire | 231,257 3 ± 0,010 9 g/mol C 62,32 %, H 6,97 %, F 24,65 %, N 6,06 %, |
| Données pharmacocinétiques | |
| Biodisponibilité | 36 % |
| Demi-vie d’élim. | 17–20 heures |
| Unités du SI et CNTP, sauf indication contraire. | |
|
modifier |
|
La dexfenfluramine, commercialisée par les laboratoires Servier sous le nom d'Isoméride ou de Redux, est une substance active médicamenteuse aux propriétés anorexigènes (effet « coupe-faim ») qui agit directement sur les récepteurs sérotoninergiques du système nerveux central.
Il s'agit d'un énantiomère S(+) de la fenfluramine, ou isomère dextrogyre de la fenfluramine. Tout comme la fenfluramine, elle fait partie de la famille des amphétamines et des phényléthylamines, d'où son effet « coupe-faim ».
Largement commercialisée dans les années 1980, elle a été retirée du marché à la fin des années 1990 en raison d'effets secondaires graves, notamment des valvulopathies cardiaques et de l'hypertension artérielle pulmonaire. Ces effets sont provoqués par la norfenfluramine, qui est un métabolite tant de la dexfenfluramine que de la fenfluramine (commercialisée sous le nom de Ponderal, Ponderax...) ou encore du benfluorex (commercialisé sous le nom de Mediator).
La recherche d'un médicament contre l'obésité
En 1918, Thomas B. Osborn et Lafayette Mendel (en) constataient que les animaux sauvages ne devenaient jamais obèses. De là datent les recherches pour trouver la substance commandant l'appétit. Si l'action anorexigène de l'amphétamine chez l'homme fut démontrée dès 1939, c'est dans les années 1960 que de nombreux médicaments anorexigènes virent le jour. On leur connaissait comme effets secondaires un phénomène d'addiction possible, ainsi que la création de psychoses.
Richard Wurtman qui avait découvert le mécanisme régulant les apports en glucides par la sérotonine, inaugura une autre voie. Avec sa femme Judith Wurtman, soutenu par le National Institute of Health, et dans le cadre du département des sciences cognitives et du cerveau du MIT, il expérimenta l'effet de la dexfenfluramine découverte dans les années 1970 et dont on connaissait les propriétés sérotoninergiques. Leurs découvertes conduisirent à un dépôt de brevet en 1980, que le MIT fut d'abord incapable d'exploiter, faute de trouver une entreprise américaine intéressée.
En 1981, le MIT passa un accord de licence avec les laboratoires Servier – qui avaient découvert les propriétés de la fenfluramine – afin de commercialiser la dexfenfluramine comme traitement de l'obésité. Les laboratoires Servier n'étant alors pas implantés aux États-Unis, le MIT et les époux Wurtman fondèrent en 1988 ou 1989 la société Interneuron Pharmaceutical Inc afin de produire la dexfenfluramine sous le nom de Redux.
On connaissait certains effets indésirables de la fenfluramine, que l'on imputait à l'isomère lévogyre. Aussi, quand les laboratoires Servier mirent au point un procédé pour séparer la forme lévogyre de la forme dextrogyre (dexfenfluramine), un traitement médicamenteux de l'obésité apparut possible (voir chiralité (chimie)#Propriétés biologiques différentes des énantiomères pour plus d'explications sur les différences entre la forme lévogyre et dextrogyre).
Autorisations de mise sur le marché et retrait
France
La dexfenfluramine obtint son autorisation de mise sur le marché (AMM) en France en 1985 sous le nom de marque Isoméride avant de l'être aux États-Unis en 1996 sous la marque Redux (1989 au Royaume-Uni et 1993 en Nouvelle-Zélande).
États-Unis
Le laboratoire Wyeth a commercialisé l'Isoméride de Servier (Dexfenfluramine) aux États-Unis.
Retrait
Censée être dénuée des effets indésirables de la fenfluramine, elle fut très largement prescrite avant d'être retirée du marché américain et français, en même temps que la fenfluramine, en septembre 1997, après l'annonce d'effets secondaires graves (valvulopathies cardiaques et hypertension artérielle pulmonaire) provoqués par ces deux substances (parfois en association avec la phentermine dans le cadre du traitement contre le surpoids dit Fen-phen (en)), tandis que son efficacité était revue à la baisse.
Le retrait a eu lieu plus tard dans d'autres pays : en Belgique, la délivrance des médicaments contenant de la fenfluramine et/ou de la dexfenfluramine (y compris les préparations magistrales) a été suspendue en novembre 1997; en Allemagne, le Bundesinstitut für Arzneimittel und Medizinprodukte (en) (BfArM) ordonne le retrait du marché le 23 septembre 1997 ; le retrait a eu lieu aussi en octobre 1997 au Royaume-Uni.
Des procédures judiciaires s'ensuivirent : très nombreuses aux États-Unis et au Canada où des class-actions eurent lieu, elles furent jusqu'à ce jour très limitées en nombre en France - pays d'origine du laboratoire Servier, détenteur des brevets - où toutefois cette « affaire de l'Isoméride » a marqué les esprits et laissé une trace dans la jurisprudence. Fin 2010, éclatait publiquement, après plusieurs années d'alertes, le scandale du Mediator, faisant également partie de la famille des fenfluramines.
L'affaire de l'Isoméride
L'Isoméride, dont le principe actif est la dexfenfluramine – c'est un chlorhydrate de dexfenfluramine– , est un médicament commercialisé dans les années 1980 comme anorexigène (médicament coupe-faim). Créé par les laboratoires Ardix, il est la propriété des laboratoires Servier. Il a obtenu son autorisation de mise sur le marché en France le puis dans 65 autres pays. Il a été considérablement utilisé en Europe et plus particulièrement en France dans les années 1980 jusqu'à son retrait du marché en 1997. Au Canada et aux États-Unis, la dexfenfluramine connut une très grande popularité dès son lancement en 1996 et ce en dépit de la controverse née en Europe qui opposa assez tôt les scientifiques concernant ses effets secondaires potentiels.
Déclenchement de l'affaire (1991-1995)
À la suite des observations effectuées en 1991 à l'hôpital Antoine-Béclère de Clamart – observations qui relèvent une coïncidence entre la consommation d'Isoméride et la survenue d'hypertension artérielle pulmonaire (HTAP) chez plusieurs malades du service – , les laboratoires Servier demandent au Pr Lucien Abenhaim, directeur du Centre d'épidémiologie clinique et de recherche en santé publique à l'université McGill de Montréal, de mener une étude internationale (International Primary Pulmonary Hypertension Study, IPPHS).
Au Royaume-Uni, dans son bulletin de juin 1992, le Committee on Safety of Medicines (en) mit en garde les médecins contre le risque d'une association entre l'administration de fenfluramine (Ponderax, Pacaps) ou de dexfenfluramine (Adifax) avec la survenue d'hypertension artérielle pulmonaire. Le comité recommandait d'en limiter la prescription à trois mois et demandait expressément aux praticiens d'exercer leur vigilance sur ce point en collaboration avec leurs patients.
Après analyse des résultats préliminaires de l’étude IPPHS qui furent connus – mais non publiés – le , des mesures de restriction d'utilisation de l'Isoméride et d'autres régulateurs de croissance à base de fenfluramines (dont le Pondéral) furent prises en France. Ainsi, le un arrêté du ministère de la Santé interdisait d'exécuter et de délivrer des préparations magistrales. Le , le directeur général de l'Agence du médicament, Didier Tabuteau, interdit la prescription en association de ces médicaments, et impose une évaluation de chaque prescription tous les trois mois. Le , le Pr Jean-Michel Alexandre, de l'Agence d'évaluation du médicament, et Jean-François Girard, directeur général de la Santé, adressent cependant une lettre aux médecins pour leur expliquer que désormais l'Isoméride ne serait prescrite qu'en contexte hospitalier.
Le , le CSP (comité des spécialités pharmaceutiques de l'Union européenne) de l'Agence européenne des médicaments (EMEA), qui avait été saisi par les autorités allemandes un an auparavant, recommanda le maintien des AMM des anorexigènes. Le comité s'inspira de l'étude IPPHS du 7 mars 1995 pour affirmer que le bilan bénéfices/risques présenté par les substances anorexigènes était favorable, sous réserve de modifier les résumés des caractéristiques des produits (RCP).
L'AMM aux États-Unis de 1996
Aux États-Unis, en revanche, la Food and Drug Administration (FDA) s'abstint, dans un premier temps, de toute mesure de précaution. En raison de la forte prévalence de l'obésité aux États-Unis, cette administration estimait que le rapport bénéfice/risque était favorable. Certes, un comité de la FDA commença par refuser, en 1995, l'homologation du Redux.
Mais, sous l'effet des actions de lobbying des associations de patients obèses comme Overeaters Anonymous ou l'American Obesity Association, relayées par certains politiciens, le , la FDA autorisa la mise sur le marché du Redux pour le traitement à long terme de l'obésité. Prise par six voix contre cinq, cette décision de la FDA a pu être influencée par un conflit d'intérêt non déclaré : deux personnes faisant partie du comité d'homologation omirent de signaler leur lien d'intérêt avec les laboratoires Servier [réf. incomplète].
La fenfluramine n'ayant une AMM que pour le traitement à court terme de l'obésité, le Redux - premier médicament autorisé pour le traitement à long terme depuis le lancement malheureux de la Dexedrine trente ans auparavant- était promis au succès dans un pays où on pouvait dénombrer 58 millions de personnes souffrant d'obésité. La mise en marché du Redux en juin s'accompagna d'une campagne médiatique d'une ampleur inhabituelle pour un médicament d'ordonnance, qui rendit peu audibles les avis divergents.
La publication de l'étude internationale IPPHS (juillet 1996)
Les résultats définitifs de l'étude IPPHS demandée par les laboratoires Servier au Pr Abenhaim furent rendus publics le . Ils mettaient en cause l'Isoméride; le Pr Abenhaïm publie aussi le dans le New England Journal of Medicine un article concernant le risque d'hypertension artérielle pulmonaire. Dans cette même édition du New England Journal of Medicine, un éditorial, signé des Drs Joann Manson et Gerald Faich, relativisait toutefois la portée de l'article du Pr Abenhaim en affirmant que les bénéfices étaient supérieurs aux risques. Les laboratoires Servier ne contestèrent pas l'étude elle-même, mais l'interprétation qui avait pu en être faite en faisant valoir que les 22 décès relevés par l'étude internationale étaient imputables à une mauvaise utilisation du médicament et non au médicament lui-même.
En novembre 1996, dans une publication destinée au grand public (FDA Consumer), les autorités américaines rapportent avoir obtenu des laboratoires qu'ils modifient les notices pour mieux y faire figurer les risques (dans l'édition de juillet-août du même magazine, la FDA mentionnait un courrier adressé par Wyeth à 300 000 professionnels de santé).
La position de la Commission européenne (1996)
Le , la Commission européenne, donnant force de loi à l'opinion exprimée le 17 juillet par le comité des spécialités pharmaceutiques, décide de modifier les règles concernant la prescription de l'Isoméride : alors que le traitement reçoit la qualification de - simple - adjuvant au régime alimentaire, sa durée doit désormais être limitée à trois mois maximum. Les modifications portent aussi sur les contre-indications, et diverses mises en garde.
1997 : les premiers procès
En mai 1997, le Boston Herald fait sa une sur le décès d'une femme de trente ans, attribué à une prescription combinée de fen-phen. En avril se tiendra le premier procès.
Le , anticipant la publication de son article prévu fin août dans le New England Journal of Medicine le Dr Heidi Connolly tint une conférence de presse à la clinique Mayo : elle y fit état de valvulopathies chez des patients ayant utilisé la fenfluramine ou la dexfenfluramine seules ou en association avec la phentermine. Ce même jour, la FDA émettait un bulletin d'alerte et avertissait par courrier plus de 700 000 médecins à qui il était demandé de faire remonter les cas qu'ils auraient à connaître. Ces évènements connurent un grand retentissement. Le , Journal Watch publiait un article fondé sur celui encore à venir de Connolly.
Fin août, la crise se précise : le 27 août, des chercheurs du National Institute of Mental Health font état de dommages observés sur les neurones d'animaux de laboratoires.Ce même jour, la FDA dans un communiqué de presse demande aux fabricants de faire figurer sur les emballages la dangerosité des mélanges fen-phen d'une part et l'existence d'un risque concernant les valves cardiaques. Toujours le 27, un haut fonctionnaire de la FDA, le Dr Michael Friedman, impute les accidents aux prescriptions hors AMM. Le 28 paraît dans le New England Journal of Medicine l'article de Connolly ; dans le même numéro un éditorial du Dr Curfman appelle à un moratoire. Enfin, le 2 septembre, lors du Congrès mondial de l'obésité, une communication porte sur les dangers des mélanges fen-phen.
Le , un procès est intenté devant une cour fédérale à Washington pour pousser les autorités à interdire la vente de dexfenfluramine ainsi que les prescriptions combinées. Le 8 septembre, la Floride proclame un moratoire sur les fen-phen. Le Tennessee avait déjà interdit les prescriptions combinées fen-phen en 1991, principalement pour prévenir les usages détournés, addictifs de la fenfluramine, mais avait dû lever cette interdiction début 1997 sous la pression de la demande et après l'adoption de mesures encadrant ces prescriptions.
Le , la FDA notifie médecins et fabricants d'un risque vasculaire chez 30 % des consommateurs de fen-phen. Ce même jour, une class action est déposée à Los Angeles. Le , la FDA demande à Interneuron et à Wyeth-Ayerst de retirer volontairement de la vente, respectivement, le Redux et le Pondimin en mentionnant les valvulopathies cardiaques, mais sans évoquer l'hypertension artérielle pulmonaire ce qui ne laissa pas d'étonner certains acteurs(de même que l'on put alors s'étonner du maintien de la phentermine).
Septembre 1997 : la suspension de l'AMM en France et le retrait de l'Isoméride par les laboratoires Servier
En France, le , l'Agence du médicament suspend l'autorisation de mise sur le marché de la dexfenfluramine (Isoméride) et de la fenfluramine (Ponderal, Pondéral longue action) en raison d’un profil de sécurité d’emploi défavorable de ces produits, qu'ils soient prescrits seuls ou en association avec la phentermine (qui n'était alors plus commercialisée en France). Servier réagit en annonçant le retrait de l'Isoméride de plus de 80 pays où il était commercialisé ; par précaution, le groupe retira aussi le Ponderal.
1997-1998 : nouvelles études
En novembre 1997, les autorités américaines recommandent à toute personne ayant pris du Pondimil ou du Redux d'entreprendre certains examens médicaux.
Début 1998, des études, réévaluant à la baisse les dommages causés par les fenfluramines, trouvèrent un grand écho dans la presse : rééxaminés suivant les standards scientifiques ordinaires, les résultats de ces études - qui s'avérèrent avoir été conduites par Wyeth - furent bientôt infirmés. En septembre 1998, la relation de causalité entre valvulopathies et dexfenfluramine ou fenfluramine fut confirmée par trois études épidémiologiques parues dans le New England Journal of Medicine. Une de ces études établissait aussi que les risques s'accroissaient avec la durée du traitement.
1999 : retrait définitif du Redux aux États-Unis
Le , le département de la Santé et des Services sociaux des États-Unis (DHHS) publia une liste de médicaments retirés définitivement du marché qui comprenait la fenfluramine hydrochloride, à savoir le Redux.
1999-2000 : la procédure française et le contentieux européen
Le , le Comité des spécialités pharmaceutiques (CSP) de l'EMEA, l'agence européenne, recommande le retrait des AMM de ces médicaments. Les laboratoires Servier déposent un recours contre cette décision le . Celui-ci est rejeté par le CSP le . Le comité recommande alors non plus seulement la suspension, mais le retrait définitif du marché de l'ensemble des médicaments anorexigènes, qu'ils soient à base de flenfluramine (ou dexfenfluramine) ou non.
À la suite de cette décision, l'Afssaps, l'agence française de sécurité sanitaire, adopta le une position intermédiaire : ordonnant la suspension d'AMM de tous les anorexigènes (ce qui était déjà fait pour les fenfluramines et dexfenfluramines), elle ne se prononça pas alors sur un retrait définitif, préférant attendre sur cette question l'avis de la Commission européenne. Le , celle-ci décide du retrait de l'ensemble des médicaments anorexigènes utilisé en santé humaine.
Cette décision de la Commission (CE (2000) 573) a été contestée par des sociétés européennes fabriquant ces produits (le 31 mai 2000 par les laboratoires Servier) : le 28 janvier 2003, un arrêt du Tribunal européen de première instance a annulé la décision de la Commission européenne du 9 mars 2000 au motif, notamment, que la Commission européenne n'avait pas compétence pour décider des AMM nationales. Le , la Commission européenne a formé un pourvoi contre l'arrêt du Tribunal de Première Instance du 28 janvier dans l'affaire T-147/00 - Servier. Ce pourvoi fut rejeté le .
En France, les AMM de la fenfluramine et de la dexfenfluramine, produits déjà suspendus du marché, ont été définitivement abrogées le .
L'étude de 2006 de Humbert et Simonneau
Début 2006, une étude rapportant les recherches d'une équipe dirigée par les Professeurs Marc Humbert et Gérald Simonneau de l'hôpital Antoine Béclère de Clamart est publiée. Celle-ci montre que les effets secondaires indésirables de certains anoréxigènes (dont la fenfluramine et la dexfenfluramine) pouvaient se manifester plus de cinq ans après la dernière prise. À la suite de cette étude, l'Affsaps dans un communiqué daté du 22 juin 2006, recommande aux personnes ayant été traitées avec un anorexigène (donc pas uniquement fenfluraminique) de consulter un médecin.
Autres
L'administration américaine souligna les dangers de certaines préparations naturelles, notamment chinoises, herbal fen-phen, vers lesquelles la consommation s'était déportée à la suite du retrait de septembre 1997.
Nota : l'association de diéthylpropion (en) et de fenfluramine a aussi pu conduire à des effets indésirables.
Mécanisme d'action
Des cas d'hypertension artérielle pulmonaire en relation avec la prise de fenfluramine avaient été rapportés dès 1981. l'hypertension pulmonaire était énumérée dans le Vidal 1992 (mise à jour avril/octobre 1992).
Le mécanisme de ces atteintes valvulaires (épaississement des valves et des cordages entraînant un défaut de coaptation responsable de fuites pouvant être importantes) serait la stimulation des récepteurs à la 5-hydroxytryptamine (ou 5-HT), présents naturellement dans le tissu valvulaire et entraînant une stimulation des mitoses et la formation d'un excès de tissu.
Le risque de développer une atteinte cardiaque s'avère, en fait, sensiblement plus faible que ce qui avait été annoncé dans les premières publications. L'arrêt du médicament entraîne une amélioration sensible mais non constante de l'atteinte valvulaire.
Au début des années 2000, des recherches américaines évoquent le rôle d'un métabolite dans l'induction des valvulopathies associées à la dexfenfluramine (tout comme à la fenfluramine) : la norfenfluramine (qui est aussi l'un des deux métabolites principaux du benfluorex).
Aspects juridiques de l'affaire
Des procès furent intentés des deux côtés de l'Atlantique. Ces actions en justice, quoique indépendantes, entretiennent des liens entre elles : ainsi, la décision des laboratoires Servier de se pourvoir en cassation était aussi motivée par le souci de ne pas offrir un argument aux associations de patients américains. De la même façon, le soin pris par les laboratoires Servier à user de leur droit de réponse chaque fois qu’une étude scientifique montrait la responsabilité de l’Isoméride pouvait s'expliquer – du moins en partie - par ce même souci de priver les parties civiles américaines et canadiennes d'éventuels arguments.
Procès au Canada
Le Redux fut introduit au Canada après avoir été introduit aux États-Unis. Le Pondéral fut retiré du marché canadien le 15 septembre 1997. Dès fin septembre, deux requêtes en recours collectif avaient été déposées dans la province du Québec concernant le Pondéral. Une troisième demande s'y ajouta bientôt tandis que deux des procédures fusionnèrent. Le 15 septembre 1998, un autre recours collectif est entrepris au sujet du Redux cette fois, contre Servier Canada Inc. Parallèlement à ces procédures, le 17 novembre 1998, des procédures en recours collectif, reliées aux produits Pondéral et Redux, sont intentées au nom de tous les consommateurs de ces mêmes produits au Canada sauf au Québec.
Le 19 octobre 2004, les juges approuvèrent les accords intervenus dans le cadre du recours collectif national (excluant les résidents du Québec) : le 29 juin 2005, ils approuvèrent ceux concernant les résidents du Québec (qui portaient sur le Pondéral et sur le Redux).
En 2000, si seulement trois affaires ont été présentées à la justice française, au Canada ce sont près de 155 000 personnes qui ont porté collectivement plainte contre la firme française Biofarma (filiale de Servier) qui fabrique les coupe-faim et contre Servier-Canada qui les distribue. Il y a eu une class action pour le Pondéral et une autre pour le Redux.
Au-delà de l'affaire elle-même, ces événements eurent un effet sur le droit lui-même. La jurisprudence, devant la multiplication des demandes de recours collectif, a dû inventer des dispositions régulant les cas de litispendance. Au Québec, ce fut le résultat de l'arrêt Servier (57Hotte c. Servier Canada inc., [1999] R.J.Q. 2598 (C.A.)), les autres provinces s'alignant sur une procédure inspirée du droit américain.
Procès aux États-Unis
En 1973, la FDA attribuait un label (une AMM) à la société A.H. Robins pour la commercialisation de la Fenfluramine. Robins fut rachetée en 1989 par American Home Products qui distribua la fenfluramine sous la marque Pondimin. Jusqu'au 15 septembre 1997, date du retrait du marché de ce produit, AHP fut le seul distributeur de ce médicament ; suivant la réglementation américaine, au titre de son AMM, AHP fut donc durant cette période la seule entité à faire remonter les cas d'effets indésirables.Les ventes du Pondimin se maintinrent à un niveau modeste jusqu'à l'année 1992, date à compter de laquelle parurent une série d'articles de Michael Weintraub dans le Journal of Clinical Pharmacology and Therapy: le Pr Weintraub y exposait les avantages de la prescription associée de fenfluramine avec la phentermine qui, d'après lui, combinait les avantages de chacune des deux substances sans en avoir les inconvénients (ce que l'on connut sous le nom de fen-phen). Les ventes de Pondimin s'accrurent considérablement : entre janvier 1995 et mi-septembre 1997, quatre millions de personnes aux États-Unis prirent du Pondimin.
Le Redux, mis sur le marché au début de l'été 1996 par American Home Products, connut un succès immédiat : six mois après son homologation, on comptait déjà aux États-Unis six millions de prescriptions pour le Redux. Entre juin 1996 et mi-septembre 1997, deux millions d'Américains en prirent.
Dès l'annonce du retrait des fenfluramines et dexfenfluramines du 15 septembre 1997, de très nombreux plaignants amorcèrent des procédures en justice. Qu'ils recherchent des dommages et intérêts s'ils estimaient avoir effectivement souffert des maux attribués aux médicaments, ou qu'il veuillent seulement obtenir les moyens de conduire des examens pour vérifier leur état de santé, ces personnes dirigèrent leurs actions d'abord et surtout contre les fabricants, mais aussi à l'encontre des médecins prescripteurs ou des centres d'amaigrissements qui avaient fait commerce de ces produits.
Ainsi plus de 2000 procès furent intentés à Interneuron. Dans les 26 mois qui suivirent le retrait des médicaments incriminés, Wyeth eut à faire face à 18 000 poursuites.
Un premier procès commença en mars 1999, qui fut interrompu par la signature d'un accord entre les parties. D'autres procès connurent la même issue : c'est seulement en août 1999 que des dommages et intérêts furent obtenus par décision d'un tribunal (23 millions de dollars). C'est après ce premier verdict que, dans le contexte d'une class action, des avocats de victimes et la société American Home Products arrivèrent à un accord (settlement agreement, Multi District Litigation, MDL 1203) définissant le cadre dans lequel les plaintes devaient être reçues et satisfaites. Le 3 janvier 2002, le terme pour les recours alternatifs ayant échu, l'accord acquit une valeur définitive. Cet accord exclut de son champ d'application l'hypertension artérielle pulmonaire (mais aussi les troubles neuropsychiatriques) : il ne concerne que les personnes pouvant faire état de valvulopathies.
Cette affaire donna lieu à la plus grande class action (civil legal action) jamais intentée : 300 000 personnes, dans leur majorité des femmes, gagnèrent contre Wyeth et Interneuron. 62 000 autres personnes ne se joignirent pas à cette procédure mais préférèrent poursuivre directement Wyeth et sa société mère, American Home Products. Exceptionnelle par le nombre de personnes qu'elle rassembla, cette class action le fut aussi par l'étendue de la fraude à laquelle elle donna lieu et ce à plusieurs niveaux.
En 2005, Wyeth - qui avait alors une capitalisation de 60 milliards de dollars - provisionna 21 milliards pour couvrir les dommages et intérêts auxquels l'exposent plus de 100 000 procès.
60 000 patients ont intenté des procès pour avoir subi des effets cardiovasculaires liés à la prise de dexfenfluramine (sous le nom de Redux) et la fenfluramine (sous le nom de Pondimin), par l'intermédiaire d'un recours collectif : 3,75 milliards de dollars d'indemnisation auraient été versés à une association regroupant 150 000 victimes afin d'éviter un procès. C'est American Home Products qui, le 8 octobre 1999, conclut un accord pour indemniser les victimes ; les indemnités se montaient à 3,5 milliards de dollars.
Le 24 janvier 2000, Interneuron attaqua en justice American Home Products au motif que cette dernière société aurait manqué de lui rapporter des informations concernant la pharmacovigilance relative au Redux.
Fait peu observé par les commentateurs, la plupart de ces class action ont suivi une voie particulière qui inverse l'ordre de la procédure : par cette reverse bifurcation, les parties se mettent d'abord d'accord sur le montant global des indemnités avant de définir le tort qui les justifie (d'ailleurs généralement, cette seconde phase n'a jamais lieu.).
Cette affaire fen-phen se déroula aux États-Unis dans un contexte politique, législatif et réglementaire qui avait poussé à l'accélération des procédures d'autorisation de mise sur le marché (Prescription Drug User Fee Act (en) (PDUFA) de 1992, sa reconduction en 1997, et la Food and Drug Administration Modernization Act (en) (FDAMA) de 1997).
Procès en France
En 1998, une femme, greffée des deux poumons, et qui avait suivi un traitement à l'Isoméride, attaque en justice les laboratoires Servier. Le , la Cour d’appel de Versailles, confirmant le jugement rendu en décembre 2000 par le Tribunal de Nanterre, condamnait les laboratoires Servier à indemniser la plaignante. Niant tout lien de causalité direct et certain entre la pathologie alléguée par la plaignante et la prise du médicament Isoméride, les laboratoires Servier se pourvurent en cassation. Dans un arrêt du 24 janvier 2006, connu sous l'appellation « arrêt Isoméride », la Cour de cassation confirmera la décision de la Cour d’appel de Versailles qui constatait la responsabilité de l’Isoméride dans la survenance d’une affection pulmonaire très grave.
Au-delà de l'affaire elle-même, la décision de la Cour d’appel de Versailles, tout comme l’arrêt de la Cour de cassation, auront des répercussions dans toute l’industrie pharmaceutique : fondant leur décision sur le droit de la consommation, les magistrats forgent une nouvelle notion du lien de causalité : il n’est plus nécessaire qu’il soit direct et certain.
À la suite de ces décisions, des actions collectives s'organisent en France, beaucoup de patients n'ayant pas été informés des effets indésirables.
Le 15 novembre 2007, la Cour d'appel de Versailles, invoquant la directive de la Communauté économique européenne N°85/374 du 25 juillet 1985, disculpait les Laboratoires Servier des charges qui lui étaient imputées en première instance. Cet arrêt fut cassé et annulé le 9 juillet 2009, par la Première chambre civile de la Cour de cassation.
Le 17 septembre 2010, un jugement du Tribunal de grande instance de Nanterre était défavorable aux Laboratoires Servier. Ceux-ci font appel du jugement.
Le 20 janvier 2011, la Cour d’appel de Versailles a confirmé le jugement rendu en 2006 par le Tribunal de Nanterre condamnant Servier à indemniser un plaignant pour le décès de sa femme, morte en 1995 d'une HTAP consécutive à la prise d'Isoméride pendant plusieurs années.
