
REGN-COV2
| Casirivimab/Imdevimab | |
| |
| Informations générales | |
|---|---|
| Princeps | Ronapreve |
| Administration | Perfusion intraveineuse |
| Laboratoire | Regeneron |
| Statut légal | |
| Statut légal | Essai clinique de phase III |
| Identification | |
| DrugBank | 15691 |
|
modifier |
|
Le REGN-COV2, ou casirivimab/imdevimab, ou Ronapreve, est un médicament développé par la société de biotechnologie américaine Regeneron Pharmaceuticals, en partenariat avec le laboratoire Roche Holding. Il s'agit d'un « cocktail d'anticorps » artificiels conçu pour produire une résistance au coronavirus SARS-CoV-2 responsable de la pandémie de COVID-19.
Principe
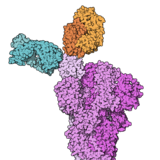
REGN-COV2 consiste en un mélange de deux anticorps monoclonaux, le casirivimab (REGN10933) et l'imdevimab (REGN10987), qui sont des copies d'anticorps produits par des patients guéris. La combinaison de deux anticorps est destinée à empêcher l'échappement de mutations.
Essais cliniques
À l'instar de l'AZD7442 d'AstraZeneca, dont le principe d'action est semblable, plusieurs essais cliniques de phase III sont en cours pour le REGN-COV2, à la fois en traitement et en prophylaxie.
Le , Roche annonce par communiqué des résultats préliminaires de phase III montrant que le traitement a permis une réduction de 70 % des hospitalisations ou des décès pour les patients à risque n'ayant pas fait l'objet d'une hospitalisation, ainsi qu'une baisse de la durée des symptômes de quatorze jours à dix jours.
Le , Roche annonce que l'étude de phase III REGN-COV 2069 a atteint ses deux objectifs, primaire et secondaire. L'administration sous-cutanée de l'association casirivimab-imdevimab a permis la réduction de 81% des infections symptomatiques chez les patients non infectés. Par ailleurs, parmi les patients malades, les symptômes ont disparu après une semaine dans le groupe traité au REGN-Cov-2 au lieu de trois semaines dans le groupe placebo .
Dans l'essai britannique Recovery, en preprint le , le REGN-Cov-2 a montré réduire la mortalité de 20% chez les patients dans l'incapacité de produire des anticorps spécifiques au Covid-19.
Le , une étude sur 1 505 personnes publiée dans The New England Journal of Medicine montre que l'administration en sous-cutané du REGN-COV2 permet une réduction de 81,4% des infections symptomatiques au Covid-19 et une réduction de 92,6% une semaine après l'injection .
Histoire
Le , Regeneron Pharmaceuticals a annoncé que le Président américain Donald Trump avait reçu « une dose unique de 8 grammes de REGN-COV2 » après avoir été testé positif pour le SARS-CoV-2. Le médicament a été fourni par la société en réponse à une demande « d'usage compassionnel » (l'équivalent de la procédure française d'autorisation temporaire d'utilisation nominative) des médecins du Président.
Le , l'EMA donne un avis favorable à l'administration du REGN-COV2 pour les patients à risque d'évolution sévère n'étant pas sous oxygène.
Mises sur le marché
Le , le Japon donne une approbation complète du Ronapreve dans le traitement des formes modérées à sévère du Covid-19. C'est le premier pays à le faire tandis que le produit est déjà autorisé dans de nombreux autres pays, mais seulement selon la procédure d'urgence .
Pour la France, le traitement est autorisé à compter du contre certaines formes graves du Covid-19.
Le , le Ronapreve reçoit l'approbation définitive de mise sur le marché en Europe par l'AEM.
Voir aussi
- Regdanvimab
- AZD7442, double anticorps monoclonal contre la COVID-19.
- Bamlanivimab, anticorps monoclonal bloquant l'entrée du coronavirus dans la cellule.
- Sotrovimab, anticoprs monoclonal humain se fixant sur la protéine Spike.