Chlorométhane
| Chlorométhane | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Structure du chlorométhane |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nom UICPA | chlorométhane | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonymes |
chlorure de méthyle |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CAS | 74-87-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NoECHA | 100.000.744 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CE | 200-817-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6327 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 36014 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILES | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | gaz incolore à odeur douceâtre | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés chimiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formule |
CH3Cl [Isomères] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse molaire | 50,488 ± 0,003 g/mol C 23,79 %, H 5,99 %, Cl 70,22 %, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° fusion | −97,6 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° ébullition | −24,2 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilité | 5 g·l-1 (eau,25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
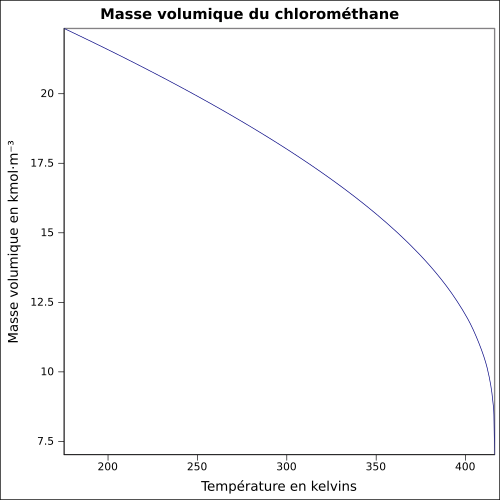
| Masse volumique |
2,306 5 g·l-1 (0 °C,1 013 mbar) équation :
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° d'auto-inflammation | 632 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limites d’explosivité dans l’air | 7,6–19 %vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pression de vapeur saturante |
4,896 bar à 20 °C 6,6 bar à 30 °C 10,9 bar à 50 °C équation :

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point critique | 143 °C, 66,7 bar, 0,353 kg·l-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point triple | −97,71 °C, 0,008 76 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermochimie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S0gaz, 1 bar | 234,36 J·K-1·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S0liquide, 1 bar | 140,08 J·K-1·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ΔfH0gaz | −83,68 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ΔfH0liquide | −102,4 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ΔfusH° | 6,431 kJ·mol-1 à 175,44 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ΔvapH° | 20,5 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cp |
81,2 J·K-1·mol-1 à 298 K équation :
équation :
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | −764,0 kJ·mol-1 (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés électroniques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1re énergie d'ionisation | 11,22 ± 0,01 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Précautions | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
H220, H351 et H373
H220 : Gaz extrêmement inflammable H351 : Susceptible de provoquer le cancer (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) H373 : Risque présumé d'effets graves pour les organes (indiquer tous les organes affectés, s'ils sont connus) à la suite d'expositions répétées ou d'une exposition prolongée (indiquer la voie d'exposition s'il est formellement prouvé qu'aucune autre voie d'exposition ne conduit au même danger) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Code Kemler : 23 : gaz inflammable Numéro ONU : 1063 : CHLORURE DE MÉTHYLE ; ou GAZ RÉFRIGÉRANT R 40 Classe : 2.1 Étiquette :  2.1 : Gaz inflammables (correspond aux groupes désignés par un F majuscule); Emballage : - |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classification du CIRC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe 3 : Inclassable quant à sa cancérogénicité pour l'Homme | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Écotoxicologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL50 | 1,8 g·kg-1 (rat, oral) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,91 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seuil de l’odorat | bas : 10 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI et CNTP, sauf indication contraire. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
modifier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Le chlorométhane, également appelé chlorure de méthyle, Fréon 40 ou R40, est un composé chimique de formule CH3Cl. Il s'agit d'un fluide frigorigène également utilisé comme réactif pour de nombreuses synthèses.
Biogenèse et présence dans la nature
Les halogénoalcanes (espèces contenant une liaison carbone-halogène) sont produits - probablement via des différents processus biologiques - par certains champignons, animaux et plantes. La molécule CH3Cl a ainsi été proposée comme un possible marqueur de vie, au cas où elle serait détectée dans des atmosphères d'exoplanètes rocheuses.
Une plante de milieux saumâtres Batis maritima produit un enzyme methyl chloride transferase qui catalyse la synthèse de CH3Cl à partir de S-adenosine-L-methionine et de chlore. Cette protéine a été purifiée, puis introduite et exprimée par génie génétique dans la bactérie E. coli. Elle semble aussi être active chez des microchampignons tels que Phellinus pomaceus, des algues rouges (ex : Endocladia muricata) ou une espèce végétale devenue localement invasive, Mesembryanthemum crystallinum, toutes connues pour aussi produire du CH3Cl. tout comme par la plante-modèle de laboratoire Arabidopsis thaliana.
Présence dans l'univers
En 2017 la molécule CH3Cl a été détectée dans et en dehors du Système solaire. D'abord par l'interféromètre ALMA autour de la proto-étoile de type solaire IRAS16293-2422, dans une zone où des planètes pourraient se former. Ensuite par le spectromètre ROSINA (à bord de la sonde Rosetta) dans la comète 67P/Tchourioumov-Guérassimenko.
La découverte de CH3Cl dans des lieux antérieurs à l'origine de la vie (connue) indique que d'autres biomarqueurs plus définitifs devront être utilisés pour conclure à la présence de vie sur d'autres planètes. Les organohalogènes pourraient par contre constituer un élément de compréhension de la chimie impliquée dans l'origine de la vie.
Propriétés physico-chimiques
Le chlorométhane est hydrolysé par l'eau à haute température pour former du méthanol CH3OH et du chlorure d'hydrogène HCl :
Cette réaction est catalysée par des composés alcalins. La réaction réciproque permet de synthétiser CH3Cl en faisant barboter du chlorure d'hydrogène dans du méthanol en présence éventuellement de chlorure de zinc ZnCl2 comme catalyseur, ou en faisant réagir du méthanol et du chlorure d'hydrogène à 350 °C sur de l'alumine Al2O3 :
À plus basse température, le chlorométhane forme un hydrate avec l'eau, ce qui pose un problème dans les systèmes de réfrigération.
Utilisation
Le chlorométhane est utilisé pour la préparation du diméthyldichlorosilane Si(CH3)2Cl2 via la synthèse de Müller-Rochow :
- 2 CH3Cl + Si → Si(CH3)2Cl2.
C'est une voie de synthèse importante pour la fabrication des silicones.
Il est aussi utilisé comme réactif pour la réaction de Wurtz-Fittig ou les réactions de Friedel-Crafts utilisée pour la production d'alkylbenzènes. C'est un réactif important pour la méthylation notamment des amines pour la formation de méthylamines quaternaires ou des groupes hydroxyles pour former de éthers.
Production et synthèse
Ce gaz est produit par chloration du méthane avec du chlore gazeux de 400 à 500 °C. Le mécanisme de chloration est une réaction radicalaire en chaîne via des radicaux issus de la dissociation du chlore. Cette dissociation peut être obtenue par voie thermique, photochimique ou par des catalyseurs. La voie thermique est préférée et elle conduit à une série de substitutions successives:
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCl4 + HCl
Le résultat de cette série de réactions est un mélange de chlorométhane, dichlorométhane, chloroforme et tétrachlorure de carbone. Ces composés sont ensuite séparés par distillation. Un excès de méthane est utilisé dans le réacteur et un recyclage est employé en présence d'un gaz inerte afin d'éviter de travailler dans un domaine où le mélange méthane-chlore est explosif.
Une autre voie de synthèse est l'hydrochloration du méthanol par du chlorure d'hydrogène. Cette réaction est actuellement privilégiée, car elle consomme du chlorure d'hydrogène, qui est un sous-produit difficile à écouler, au lieu d'en produire comme dans le cas de la chloration. De plus la synthèse conduit à la seule production du chlorométhane et évite la production des composés multichlorés.
Toxicologie
Il existe un faible nombre d'études, souvent anciennes, chez l'homme. De plus, le chlorométhane étant souvent utilisé conjointement à d'autres produits, il est difficile de déduire l'effet spécifique de la molécule à partir de l'observation d'un groupe (voir la fiche toxicologique de l'INRS ).
Ceci a amené le CIRC à classer le chlorométhane dans le groupe 3 quant à son aspect cancérigène du fait du peu de données. Les études disponibles ont néanmoins amené le chlorométhane à être classifié (selon la classification SGH) comme étant :
H351 - Susceptible de provoquer le cancer
H373 - Risque présumé d'effets graves pour les organes à la suite d'expositions répétées ou d'une exposition prolongée
Effets métaboliques
Plusieurs études pointent différents risques rapportés par l'INRS :
Il est ainsi rapporté une rapide absorption chez l'animal et chez l'homme par voie respiratoire .
Chez la souris une exposition chronique entraine des dégénérescences dans la couche granuleuse du cortex à partir d'une exposition de 100 ppm
Un second protocole, testé chez le rat et la souris, rapporte des dégénérescences au niveau des reins, du foie, des glandes surrénales et du cervelet ainsi que des pertes de coordination des membres antérieurs, une paralysie des membres postérieurs, des convulsions et des diarrhées en fonctions des concentrations testées. Les souris y étant plus sensibles que les rats. Une divergence des effets a été observée en fonction du sexe (dégénérescences du cervelet chez les femelles et nécrose hépatique chez les mâles).
Chez l'homme, les études sont souvent anciennes et apportent parfois des résultats contradictoires. Les effets d'une exposition importante au chlorométhane semblent principalement être des affections du système nerveux central (signes neurologiques (syndrome cérébelleux, somnolence, apathie, troubles de la vision, perte de mémoire à court terme, confusion, perte de conscience). On observe également des troubles digestifs (nausées, vomissements, douleurs abdominales, diarrhées), une asthénie et des céphalées. Les symptômes peuvent persister plusieurs mois et des séquelles neurologiques et/ou psychiatriques sont possibles. Plusieurs cas de décès sont rapportés, mais sans indication sur les concentrations. En cas de forte exposition, des effets cardiaques et rénaux sont observés .
L'exposition chronique aux doses usuelles n'a fait l'objet que de très peu d'études ou d'études uniquement anciennes. Dans les études publiées les effets sont rarement observables et lorsqu'ils le sont (troubles de l'équilibre, de la vision et de la mémoire, une fatigue, des étourdissements et des signes de confusion) ils ont été observés comme étant réversibles .
Effets génotoxiques
Le chlorométhane est génotoxique pour les bactéries et cellules de mammifères in-vitro. Toutefois in-vivo, les effets de réparations de l'ADN viennent compenser et ces effets ne sont pas observés dans les rares études existantes.
Effets cancérigènes
Chez le rat les protocoles testés ne montrent aucun effet cancérigène observable mais chez la souris des tumeurs rénales sont observées.
Les données chez l'homme sont insuffisantes et la co-exposition avec d'autres produits complique l'interprétation des données existantes .
Effets sur la fertilité et tératogènes
Chez le rat et chez la souris des effets sur la fertilité et sur la santé des fœtus ont été observés. Une baisse de la fertilité des mâles a ainsi été observé chez les rats soumis à une exposition chronique de chlorométhane . Les effets sur les fœtus chez la rate ne sont observable qu'a forte dose avec le protocole testé toutefois chez la souris des effets de malformation du fœtus dont observées dès les plus faibles doses testées .
Aucune donnée n'existe chez l'homme .